Metabolismo de las proteínas; alimentos y aminoácidos esenciales

Las proteínas son moléculas orgánicas de gran tamaño formadas por largas cadenas lineales de aminoácidos. Las proteínas desempeñan gran cantidad de funciones en el organismo, son el principal componente estructural de las células y tejidos del organismo, siendo indispensables para su correcto funcionamiento. A través de la dieta se obtienen los aminoácidos que el cuerpo no es capaz de sintetizar por sí solo, los aminoácidos esenciales. El aporte de proteínas en la dieta debe suponer 10-15% del aporte calórico diario total.
Las proteínas son macromoléculas formadas por largas cadenas de aminoácidos que desempeñan múltiples funciones en el organismo. Proporcionan nitrógeno y aminoácidos que el cuerpo utilizará para la síntesis y el mantenimiento de las proteínas codificadas en el genoma. De las proteínas también se obtienen sustancias nitrogenadas metabólicamente activas como hormonas, ácidos nucleicos, neurotransmisores, creatina o glutatión; además el esqueleto carbonado de los aminoácidos se utiliza en diferentes vías metabólicas o como sustrato energético (1).

Las proteínas están formadas a partir de 20 aminoácidos, denominados proteinógenos, permitiendo que existan posibilidades prácticamente infinitas de polímeros. Las proteínas pueden desempeñar diversas funciones: catalítica (enzimas), reguladora (hormonas o neurotransmisores), transporte (albumina o las apoproteínas), estructural (colágeno), defensiva (inmunoglobulinas), de reserva (ferritina), y, finalmente, energética (2).
Clasificación de los aminoácidos
Los aminoácidos se pueden clasificar de diversas maneras: por su estructura, según la carga de la cadena lateral o desde el punto de vista nutricional. Esta última forma de clasificarlos los divide en esenciales y no esenciales. Los aminoácidos esenciales son aquellos que el organismo no es capaz de sintetizar, por lo que deberán de ser aportados en la dieta. Por otro lado, hay un grupo de 8 aminoácidos que serán esenciales sólo en determinadas situaciones, como en casos de malnutrición o tras una cirugía, que se denominan aminoácidos condicionalmente esenciales (2).
| Esenciales | Condicionalmente esenciales | No esenciales |
|---|---|---|
| Leucina | Prolina | Glutamato |
| Isoleucina | Serina | Alanina |
| Valina | Arginina | Aspartato |
| Triptófano | Tirosina | |
| Fenilalanina | Cisteína | |
| Metionina | Taurina | |
| Treonina | Glicina | |
| Lisina | Glutamina | |
| Histidina |
Calidad de las proteínas y fuentes dietéticas
La calidad de las proteínas varía en función de su digestibilidad y composición en aminoácidos. Teniendo en cuenta estos parámetros, las proteínas de un alimento serán de mayor o menor calidad en función del aporte de aminoácidos que necesita el organismo. Esta capacidad de aportar los aminoácidos necesarios se define como el valor o calidad biológica (2).
Los parámetros biológicos de mayor utilidad para valorar la calidad proteica de los alimentos son tres. El coeficiente de digestibilidad informa de la utilización digestiva de la proteína ya que establece el porcentaje de proteína absorbida respecto a la ingerida. Por otro lado, el valor biológico indica la utilización metabólica de los aminoácidos absorbidos, dando el porcentaje de nitrógeno retenido con respecto al absorbido (2). Se utilizan como proteínas de referencia las del huevo o de la leche humana, que tienen un valor biológico entre 0,9 y 1 (1). Finalmente, el coeficiente de utilización neta de la proteína refleja las pérdidas de nitrógeno en la digestión, dando así una visión global de la proteína incorporada en el organismo en relación a la que se ha ingerido (2).
Según la Encuesta Nacional de Ingesta Dietética (ENIDE), la mayor parte de la proteína, casi el 80% de la dieta, procede de alimentos de origen animal, distribuyéndose de la siguiente manera: carne 31%, pescados 27%, huevos 11% y lácteos 10% (4).
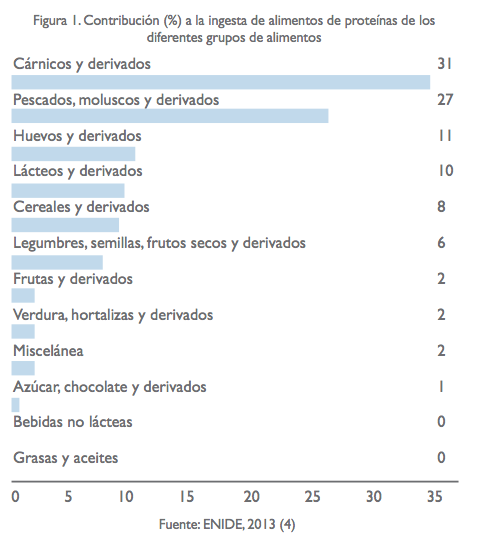
Los alimentos de origen animal, como la carne, el pescado, los huevos y la leche y sus derivados, contienen prácticamente todos los aminoácidos esenciales, por lo que son considerados alimentos proteicos de alta calidad. Por otro lado, los alimentos de origen vegetal se consideran de menor calidad ya que pueden ser deficitarios en uno o varios aminoácidos o por su menor digestibilidad. Dentro de los alimentos de origen vegetal, el pan y otros productos a base de cereales, las legumbres y los frutos secos, son los productos con mayor cantidad de proteínas (1).
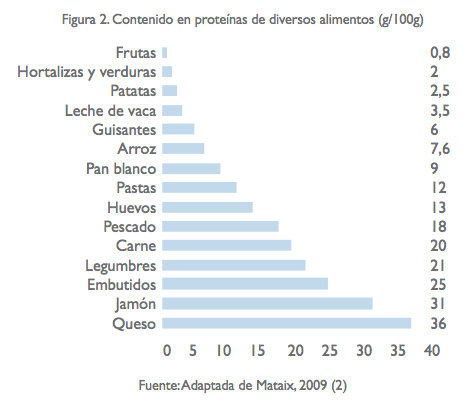
Normalmente se mezclan alimentos con diferente composición proteica por lo que no se debe considerar la proteína de un alimento de forma aislada. La complementación proteica resulta de la combinación de alimentos con proteína de baja calidad que se complementan en aminoácidos esenciales dando una composición proteica de mayor calidad. De forma general se podría decir que los alimentos de origen animal, a excepción del huevo y las legumbres, son deficitarias en metionina, mientras que los vegetales lo serían en lisina (2). Además de estos aminoácidos, también pueden ser limitantes la treonina y el triptófano (5).
| Legumbres | Cereales integrales |
| Legumbres | Frutos secos y semillas |
| Legumbres | Bebidas vegetales (avena o arroz) |
| Cereales integrales | Frutos secos y semillas |
| Cereales integrales | Bebidas vegetales (soja) |
| Frutos secos | Bebidas vegetales (soja, avena, arroz) |
Fuente: Vidal García E. 2009 (5)
Metabolismo de las proteínas
En el metabolismo de las proteínas se incluyen aquellos procesos que regulan la digestión de las proteínas, el metabolismo de los aminoácidos y el turnover de las proteínas; procesos que a su vez incluyen la absorción y suministro de aminoácidos de la dieta, la síntesis de novo y utilización de aminoácidos y la hidrólisis y síntesis de proteínas (1). Las proteínas, al contrario que otras biomoléculas, no se almacenan. Todos los aminoácidos, ya sean de la dieta como derivados del turnover, se degradan. Los aminoácidos se metabolizan mediante la escisión, por un lado de su esqueleto carbonado y por otro lado del grupo amino, este último se eliminará en forma de urea (2).
La digestión de las proteínas comienza en el estómago, donde serán atacadas por la enzima pepsina, y se completa en el duodeno y yeyuno. El jugo pancreático, junto con las enzimas que contienen las células intestinales, transformarán el contenido proteico en estructuras más simples. Estas pasarán a través de la mucosa intestinal hasta llegar a los enterocitos donde se completará la hidrólisis, obteniendo así aminoácidos y, en una menor cantidad, oligopéptidos (2).
Para entrar en el enterocito desde la luz intestinal, hay dos tipos de sistemas de transporte, unos dependientes de sodio y otros independientes de él, tratándose de sistemas de transporte activo con gasto energético. Una vez dentro del enterocito, los aminoácidos obtenidos pueden seguir varias vías metabólicas. Estos podrán ser utilizados para obtener energía o para la síntesis de proteínas para el propio enterocito o se liberarán directamente a la sangre portal para su posterior utilización por parte de los diferentes tejidos. La glutamina, el aspartato y el glutamato son la principal fuente de energía del intestino y aproximadamente el 10% de los aminoácidos absorbidos están destinados a la síntesis proteica endógena en el enterocito. En la mucosa también se realizan algunas transformaciones, especialmente la transaminación del aspartato y del glutamato. Debido a esta transaminación no hay grandes cantidades de estos aminoácidos en sangre, por lo que encontramos el producto derivado de la transaminación, la alanina. (2).
El metabolismo proteico en hígado y músculo, al contrario que en el enterocito, está sujeto a control hormonal. Los aminoácidos llegan al hígado por la vena porta, donde parte de ellos podrán ser liberados a la circulación sistémica y otros utilizados para la síntesis de proteínas (como albumina, transferrina, fibrinógeno etc.) u otros derivados metabólicos nitrogenados (como purinas y pirimidina) o catabolizarse para producir energía. La utilización de aminoácidos para obtener energía solo se produce en casos en los que la ingesta es muy rica en proteínas; en casos normales estos se utilizarán para la síntesis de proteínas y otros compuestos nitrogenados. Los aminoácidos libres serán transportados por sangre hasta las células de los diferentes tejidos (2).
En la degradación de aminoácidos se produce amoniaco que, al ser una sustancia muy tóxica, se debe transformar en urea, que será eliminada por el riñón. El amoniaco se produce en dos etapas: en primer lugar se produce una transaminación con formación de glutamato y, posteriormente, se realiza una desaminación del glutamato con formación de amoniaco (2). El esqueleto carbonado restante, dependiendo de las condiciones fisiológicas, podrá ser utilizado para la obtención de energía o se trasformará en glucosa (gluconeogénesis).
Los aminoácidos se pierden de forma irreversible por las heces, por oxidación metabólica y por la orina. Además, también se producen pérdidas por el pelo, la piel, secreciones bronquiales y en la leche de las mujeres en periodo de lactancia (2).
Requerimientos de las proteínas
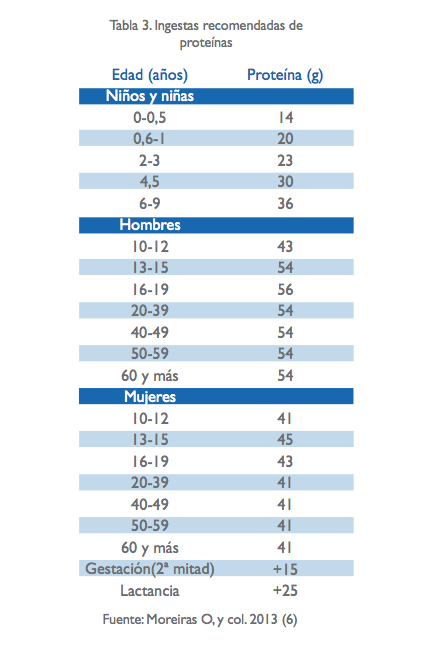
Las necesidades proteicas de un adulto son de 0,8 g/kg/ día, lo que supone el 10-15% del aporte calórico diario total. Del total de las proteínas de la dieta, se recomienda que el 50% de estas sean de origen animal y el otro 50% de origen vegetal. Las necesidades en proteínas varían a lo largo de la vida: los bebés, los niños y los adolescentes las necesitan para crecer, las gestantes para el correcto desarrollo del feto y las lactantes para la producción de leche, por lo que tendrán unas necesidades mayores que las de un adulto medio (5).
Referencias
- EFSA Panel on Dietetic Products, Nutrition, and Allergies. Scientific Opinion on Dietary Reference Values for protein. EFSA Journal 2012;10(2):2557.
- Mataix Verdú J. Nutrición y Alimentación Humana. Manual teórico práctico 2a Ed. Madrid: Ergon; 2009.
- Vázquez C, De Cos A.I, López-Nomdedeu C. Alimentación y Nutrición. 2a Ed. Madrid: Díaz de Santos; 2005.
- Agencia Española de Seguridad Alimentaria y Nutrición. Evaluación nutricional de la dieta española I. Energía y macronutrientes. Sobre datos de la Encuesta Nacional de Ingesta Dietética (ENIDE). Ministerio de Sanidad, Servicios Sociales e Igualdad, 2013.
- Vidal García E. Manual Práctico de Nutrición y Dietoterapia. Ed. Monsa Prayma: Barcelona; 2009.
- Moreiras O, Carbajal A, y col. Tablas de composición de alimentos. Guía de prácticas. 16a ed. Madrid: Ediciones Pirámide; 2013.
Categoria
Nutrición básicaTe recomendamos
Legislación de los alimentos ecológicos en la UE

de Eroski Consumer
“No hay información sobre las sustancias que están en nuestro entorno ni se han considerado las sinergias o interacciones que pueden provocar”

de Eroski Consumer
Los cereales en la dieta

sobre Proteínas
Los otros cereales

sobre Proteínas








Añadir nuevo comentario